임상뼈 생물학의 핵심
본지는 지난호부터 12회에 걸쳐 권경환 교수의 임상원고를 게재하려고 한다. 임플란트식립과 악교정 및 안면성형수술을 하면서 치과임상에서 뼈의 중요성은 점점 더 증가하고 있다. 따라서 임상적인 입장에서 뼈 생물학을 다시 돌아보는 기회를 갖고자 한다. 또한, 뼈의 구조와 뼈의 세포학적인 내용과 뼈 성장인자에 대한 내용 등을 함께 정리하는 기회로 마련코자 한다. (편집자주)
뼈를 구성하는 피질골과 골수강은 상호보완적인 관계를 이루고 있으며 이러한 상호보완관계에 따라 골재생의 순환구조를 형성하게 된다. 이러한 순환구조에서 중심적인 역할을 하는 사이톸카인중에 Bone morphogenetic protein-2(BMP-2)가 있다.
(1) rhBMP-2는 화학주성과 분화, 증식 작용을 하는 중심역할을 한다.
골형성단백질은 화학주성(chemotatic) 속성을 보여주고 있으며 미분화세포를 골모세포와 골세포, 연골세포(chondroblastic line) 세포로 분화되고 유도하는 다양한 세포 유형으로 증식효과를 갖고 있다(Reddi & Cunningham, 1993).
더욱이, BMPs는 강력한 골유도 활성을 보이고 있다(Hogan, 1996; Rosen et al., 1996). 이 단백질의 광범위한 계열의 구성원 중 BMP-2, 4 및 7은 골 형성 과정에 중요한 역할을 한다는 것이 증명된바 있다 (Hogan,Rosen et al.). 재조합 인간 골형성단백질은 최근에 두가지 방법으로 재조합 방법을 소개하고 있는데 Cho cell line이라고 하는 Chinese hamster ovary cells(CHO cells)로 골형성단백질을 재조합하여 생산하는 방법이 있고 대장균 세균총인 E coli를 이용한 재조합과정을 거치는 방법이 있다. 이와 같이 재조합 인간 골형성 단백질은 골재생 골유도능에서는 약간의 차이가 존재하지만 임상적인 큰 차이를 나타낼 정도는 아닌 것으로 증명되고 있다.
1965년에 Marshall Urist는 비골 부위(nonbone site)에 탈회된 골 매개체(matrix)가 연골 조직과 새로운 뼈 형성을 유도한다는 것을 발견한 바 있다(Urist, 1965).
Urist는 이 과정을 자가유도(autinduction)로 정의하고 나중에 단백질 추출물이 탈회뼈와 분리되어 새로운 뼈 형성을 일으킨다는 사실을 보여 주었다 (Urist et al., 1973). 이 모델에서는 새로운 뼈 형성 전에 연골 조직 형성과 함께 연골 내 골화를 특징으로 하는 상태를 발생하게 되고이후에 새로운 뼈가 형성되었다 (Urist et al., 1979; Sampath & Reddi, 1981).
BMP-2는 뼈를 형성하는데 중심적인 역할을 수행하고 있지만 인공적으로 주입시에 빠른 흡수와 고농도로 주입하는 것보다는 저농도로 3주 이상의 유지가 골형성에는 뚜렷한 효과를 나타내는 것으로 나타났다. 이러한 저농도 3주 이상의 유지를 위한 scaffold의 개발이 무엇보다 시급한 실정이다. 최근 연구에 있어서 가장 근접한 scaffold로는 LFA collagen(Lidocaine-Fibrinogen-Aprotinin collagen)이 가장 근접한 scaffold는 각광을 받고 있다.
(2) 골수는 Osteon을 만드는 저장창고입니다.
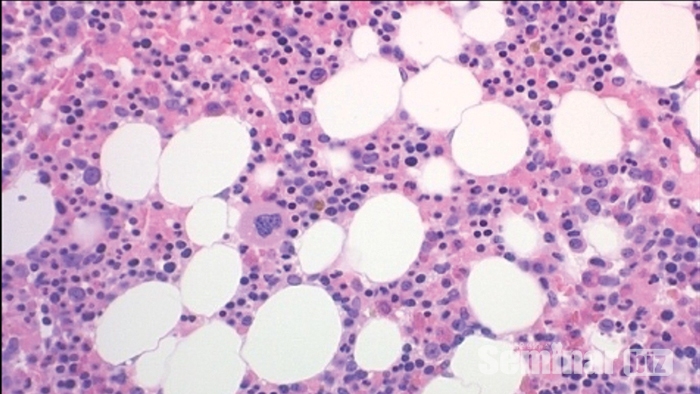
골수는 뼈의 중심인 골수강에서 발견된다. 골수는 순환하는 혈액 세포가 생성되는 곳으로 (조혈 (hemematopoiesis)로 알려진 과정) 조기에 인간의 삶에서 많은 뼈에 발생하지만, 발달 중에는 조혈이 심하게 뼈에 집중되어 사춘기가 되면 주로 흉골, 척추, 장골 및 늑골에서 혈액이 생성된다. 조혈을 겪고 있는 골수는 적혈구의 존재로 인해 적색으로 착색되지만, 조혈을 겪지 않는 골수는 황색으로 나타난다. 적색 골수는 스폰지 모양의 망상 골격 내에서 긴 골반 (빔 모양의 구조)으로 이루어져 있다. 이 골격 주위의 공간은 지방 세포, 간질 섬유 아세포 및 혈액 세포 전구체로 채워져 있다. 건강한 골수 생검은 Figure9-1에 나와 있다.
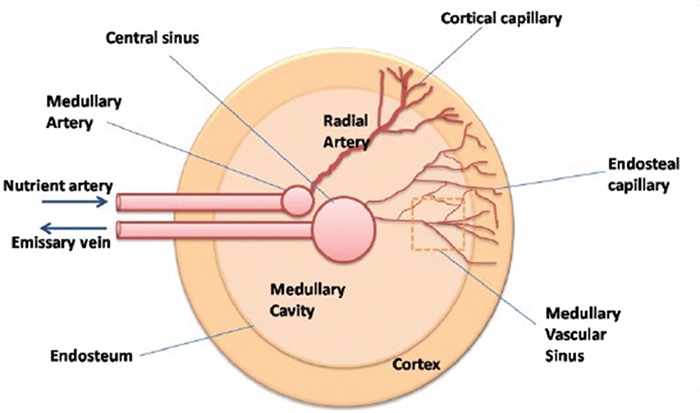
혈액 세포가 발생하는 동안, 이들 조혈 전구 세포는 골수 내 영역 (내 뼈 표면)에서 중심 영역으로 이동한다 (Figure 9-2).
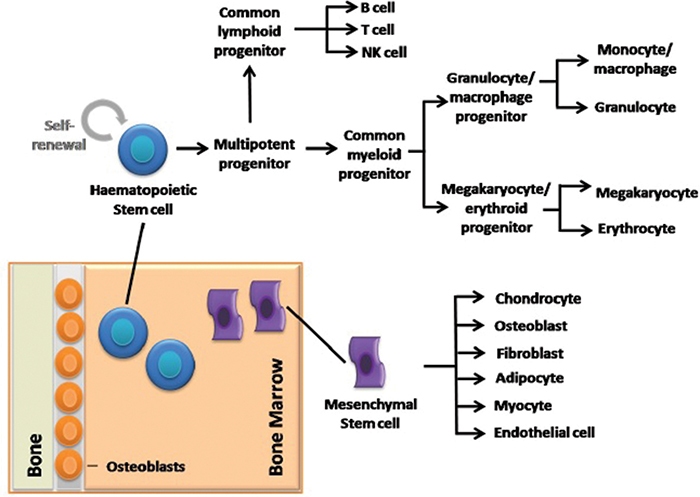
성숙한 혈액 세포는 혈관동(vascular sinus)의 고밀도 네트워크를 통해 빠져 나온다. 조혈 중에는 조혈 줄기 세포 (haematopoiesis the haematopoietic stem cells, HSC)가 분열되고 HSC 풀을 계속 갱신하기 위해 하나의 딸 세포(daughter cell)가 골수에 남아 있다. 다른 딸 세포는 성숙한 혈액 세포가 되고 순환에 들어가기 위해 골수를 떠나기 위해 여러 단계의 발달 단계를 거치게 된다 (Figure 9-4 참조). Mesenchymal 줄기 세포 (Mesenchymal stem cells, MSC)는 골수강에서 발견되며 연골 세포 (연골 생성), 골아 세포 (뼈 형성), 지방세포 (지방), 근육 세포 (근육), 내피 세포 및 섬유 아세포와 같은 다수의 간질 계통으로 분화된다.
골수강을 유지하고 있는 조혈줄기세포와 다양한 딸 세포들은 피질골을 구성하는 osteocyte의 osteon을 형성하게 된다.
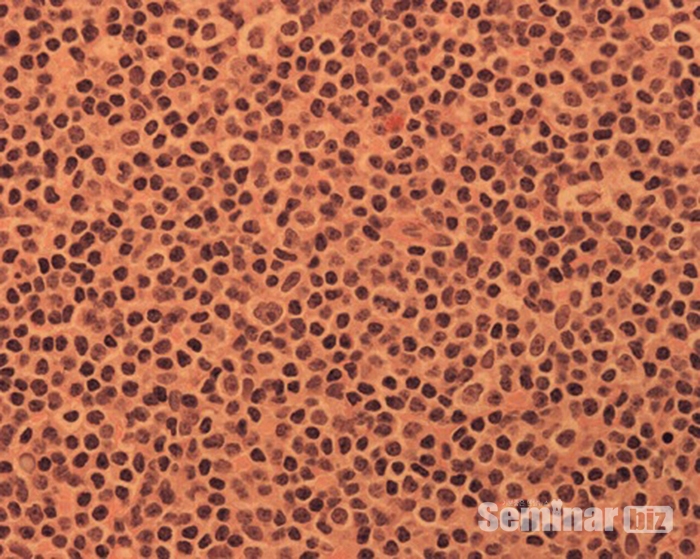
골수강과 피질골간의 상호관계가 깨지게 되는 경우 골수염이나 피질골염이 발생되게 되고 이러한 현상으로 염증성 증상이나. 골괴사증과 같은 양상이 나타나게 된다. 골수를 떠나 더 발전된 후에, 활성화된 항원-경험 B 세포 (activated antigen-experienced B cells) 는 형질 전환 세포 (Plasma Cell) 로 분화되어 골수강내에 세력화하게 된다.
분비된 사이토카인 및 세포 표면 수용체와 함께 골수 및 그 안에 존재하는 모든 세포의 골격은 복잡한 미세 환경을 구성한다. 이 미세 환경의 유지는 조혈, 세포 발달을 촉진하고 혈액학적 질환을 예방하는 데 중요하다.
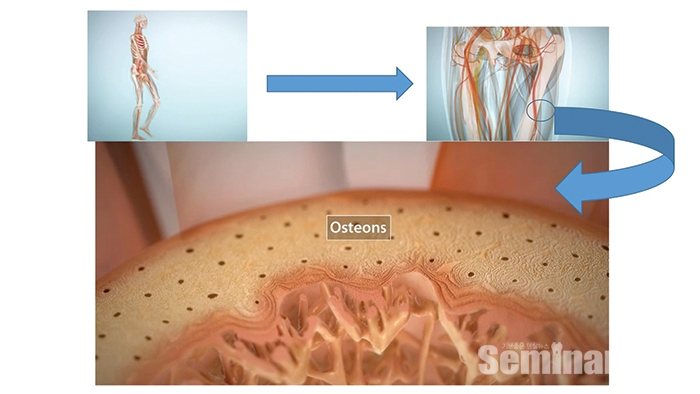
(3) 피질골의 기본은 Osteon으로 구성되어 있다
(Figure 9-6, Figure 9-7)
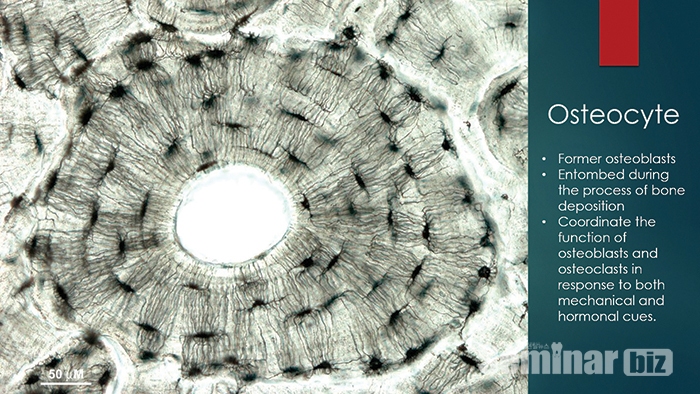

Osteon은 작고 굵은 피질의 주요 구조 단위로, 긴 동공 통로를 둘러싸고 있는 얇은 판 (lamellae)이라고 불리는 동심원의 뼈 층으로 이루어진 Haversian‘s canal (17 세기 영국의사인 Clopton Havers의 이름을 딴 것)이다.
Haversian canal은 골세포에 혈액 공급을 담당하는 작은 혈관을 포함한다. Osteons은 길이가 수 밀리미터이고 지름이 약 0.2 밀리미터 (0.008 인치)이다. Haversian canal은 뼈의 긴축(long axis) 과 평행하게 움직이는 경향이 있다.
Osteons는 성숙한 뼈의 특징이며 뼈의 신생 또는 재생 과정에서 형태를 취하게 된다. Haversian canal 근처의 osteoclasts 큰 세포에 의해 미숙한 osteocyte와 성숙 osteocyte를 파괴하면서 재생과정이 진행된다.
뼈를 형성하는 세포 또는 골아 세포의 층은 파골 세포를 따라 가고 canal의 측면에 새로운 뼈를 생성하게 된다. 이렇듯 골이식이나 골재생은 기존의 osteocyte와 osteon을 파괴하고 새롭게 형성된 canal주변에 osteoblast가 이동해서 osteon을 형성하게 된다.
피질의 장축에 수직으로 가로 지르는 횡단 혈관을 Volkmann canal라고 부른다. Volkmann canal은 인접한 osteons를 연결하고 또한 Haversian canal의 혈관을 골막의 외면을 덮는 조직인 골막과 연결시키는 역할을 한다.
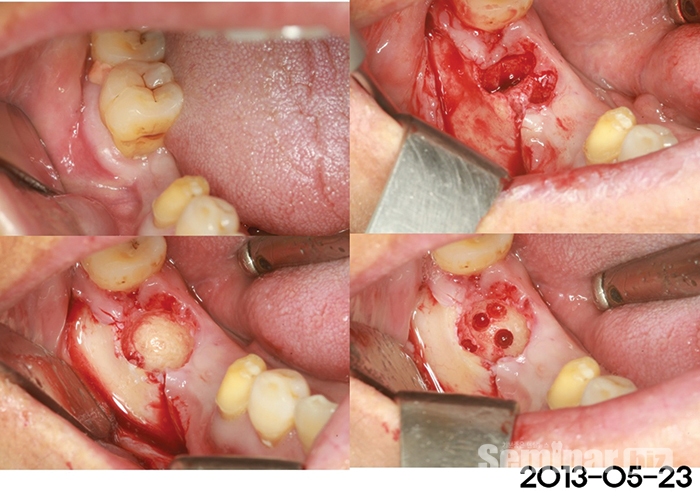
골이식이나 골재생시에 Haversian canal과 Volkman canal간의 연결되어 있는 부분을 활성화시키기 위해 골막천공이나 골수내 천공 시술을 통해 혈관화를 촉진시키는 방법이 이용되기도 한다(Figure 9-8).
다음 호에 계속 ▶

